原标题:康方生物港股上市开始申购,双抗差异化竞争突破PD-1治疗瓶颈
康方生物开始申购,港交所将再度迎来中国创新药企业。
尽管前一段时间受疫情的影响,二级市场大环境形势不佳,但是医药板块仍然保持着自己的强劲势头,多家企业逆势上涨。最近上市的诺诚健华,股价也在上市后持续上涨,如今总市值已经超过了150亿港币。
如今大盘形势转暖,康方生物本次上市可能也会更加顺利。我们通过研究康方生物的招股说明书和相关资料,总结出康方生物的以下特点:
1、主创团队长期从事医药领域研发工作,多名成员曾一起共事,团队默契程度高;
2、摩根士丹利和摩根大通联席保荐;
3、多家机构持续增资,D轮融资1.5亿美元,估值近60亿;
4、与多家国内外药企达成合作,曾将产品授权给默沙东;
4、独创ACE平台管控新药研发全流程,TETRABODY技术解决生物药研发难点;
5、两款头部产品即将申报上市,AK-104(PD-1/CTLA-4)突破免疫治疗有效率瓶颈;
6、后续产品管线充足,控制新药研发风险;
7、研发开支持续增长,现金储备充足但负债率较高。
优质团队引得资本关注
康方生物是一家临床阶段生物制药公司,由免疫学专家海归创业团队于2012年3月创建成立。致力于自主发现、开发及商业化首创及同类最佳疗法。公司的愿景是成为一家在开发、生产及商业化病人可负担的下一代创新治疗性抗体方面,处于全球领先地位的企业。
康方生物创始人夏瑜博士拥有20余年学术界和生物制药工业界的从业经历,在中山大学取得了生物化学学士学位和硕士学位之后,去往英国纽卡斯大学获得分子生物学和微生物学博士学位,并随后在英国格拉斯哥大学和美国路易斯尔大学医学院从事了生物化学、免疫学及癌症免疫疗法的研究。
在研究生涯之后,夏瑜博士进入药企从事临床前研究、工艺开发、工艺放大、技术转化甚至抗体GMP生产等一系列工作,曾任职于拜耳、PDL生物制药(现雅培制药)、Celera Genomics等公司。2008年,夏瑜回国加入中美冠科担任高级副总裁,同时兼任太仓冠科总经理,并兼任辉瑞-冠科亚洲癌症研究中心冠科负责人。
康方生物的高管成员大多都已经从事了十几年的医药领域工作,在自己的专业领域有丰富的经验。如首席科学家李百勇博士、高级副总裁王忠民博士、副总裁张鹏博士,都曾与夏瑜在太仓冠科共事。因此康方生物团队成员彼此之间已经有了工作上的默契,也让康方生物在过去8年中的发展顺风顺水。
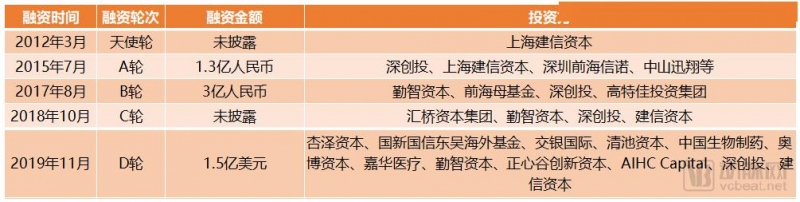
康方生物上市前融资历程
在优质团队的加持下,2012年3月,刚刚成立的康方生物就获得了上海建信资本的天使轮投资。2015年7月,公司完成了人民币1.3亿元的A轮融资,投资方包括深创投、上海建信资本。随后,这几家机构一直伴随着康方生物的成长,在后续的融资轮次中屡次增资。A轮时,康方生物的估值只有约3.3亿元人民币。到2019年底的D轮时,康方生物的估值折合人民币就已达到了58.2亿元(8.36亿美元),在短短的四年内增长了16倍。
凭借着自身的研发能力,康方生物屡次与大型制药企业达成合作。2015年,康方生物将自主研发的肿瘤免疫治疗抗体药物AK107授权给了制药巨头默沙东;2016年,康方生物又与东瑞医药成立合资公司,共同开发AK102和AK109;2018年,与GE合作,建立华南地区第一家采用GE FlexFactory技术的生物制剂生产车间;2019年,与中国生物制药公司旗下的正大天晴制药集团有限公司签订合营协议,共同开发及商业化AK105(Penpulimab)。
独特TETRABODY技术解决双抗研发问题
康方生物对自己的研发实力非常有自信。他们相信,自己完全集成的内部研发能力对他们在中国的成功至关重要。
ACE平台
在成立之初,康方生物就开发出了一套管理体系,称为康方全方位探索平台(ACE平台)。ACE平台涵盖了全方位现代生物药发现、研究和工艺研发,帮助康方生物在极少依赖外部供应商的情况下营运。
根据工作重点,康方生物对ACE平台的每个功能进行了特别优化,着重关注候选药物生命周期中各关键节点上建立跨功能集成。ACE平台保证了不同职能小组能在同一候选药物的生命周期关键节点上顺畅协作,提高开发速度和成功的可能性,同时降低开发成本。
在研发环节上,康方生物的核心技术在于其TETRABODY技术,以及在晶体学和基于结构的抗体设计及工程方面的专业相关知识。
TETRABODY技术平台能帮助康方生物克服在开发和生产双特异性抗体中遇到的三项反复发生的CMC难题,包括由于双特异性抗体的高分子量导致的低效表达水平、双特异性抗体的结构异质引起的工艺开发障碍以及由于双特异性抗体缺乏稳定性而导致的药物不良性。
针对这些常见问题,TETRABODY技术可以优化构架格式及连接序列,实现更高的稳定性和表达水平;对称形状带来均质性和更好的稳定性;以及四价设计提高活性和临床疗效。
核心产品已开启关键临床试验
经过8年的发展,康方生物已经建立起一组以肿瘤学和免疫学药物为核心的药物研发管线。其中两款头部产品,AK104和AK105已确定进入关键临床阶段,多项适应症将在2020-2021年逐步申报上市。另外四款产品也已确定进入临床试验阶段,此外还有多款临床前产品在研。
康方生物在研管线列表
1.AK104:PD-1/CTLA-4双特异性抗体宫颈癌适应症已进入关键期临床试验
康方生物的主力产品AK104,是一种针对PD-1/CTLA-4双靶点的双特异性抗体,商业化权利由康方生物95%控股的康方药业持有。
CTLA-4和PD-1一样,也是活化T细胞表面表达的免疫检查点分子。在免疫治疗领域中,CTLA-4是除了PD-1/PD-L1以外,最热门的免疫治疗靶点。目前获批上市的只有百时美施贵宝(以下简称BMS)的Yervoy(通用名Ipilimumab)。该药也是第一款获批上市的免疫治疗药物,用于治疗黑色素瘤。该药在2019年全球销量达到14.89亿美元,虽然也已达到了重磅炸弹级别,但是相比于其他免疫治疗领域的明星药物,如Keytruda超百亿美元的销量,其表现并不算强势。
目前对于CTLA-4靶点的开发,主要在于CTLA-4单抗与PD-1单抗的联合治疗。BMS就针对自己旗下的两款产品Vervoy和Opdivo,在食管癌、膀胱癌、胃癌、头颈癌等多个不同癌种中布局了多项临床试验。目前为止的临床试验结果显示,联合治疗确实对PD-1单抗的治疗效果起到了促进作用,但是另一方面,患者的不良反应发生率也发生了明显上升。
康方生物研发的AK104可能会是更好的治疗方案。AK104可以同时靶向PD-1和CTLA-4两个靶点,起到与联合治疗同等的治疗效果,目前的临床试验结果也基本证实了这一点。
截至2020年2月26日,在AK104单药治疗选定实体瘤的研究队列中,数据统计的33名受试者中,有7名受试者实现部分缓解(PR),16名受试者病情稳定,ORR达到21.2%;在另一项AK104联合mXELOX(奥沙利铂联合卡培他滨方案)治疗胃癌和食道腺癌的研究中,16位受试者中的10位实现部分缓解(PR),客观缓解率达62.5%。这些数据都表现出AK104在疗效上的潜力。
同时相比于联合治疗,单药治疗的安全性大为提升。在184名接受AK104治疗的患者中,≥3级TRAE(与治疗相关的严重不良事件发生率)只有13%,即使在最高剂量的450mg组,这一数据也只有18%。而在研究Opdivo和Vervoy联合治疗的checkmate系列试验中,≥3级TRAE在最低的Checkmate-227试验中也达到了33%,最高的Checkmate-067试验中更是达到了59%。
AK104临床研究计划
目前康方生物已经针对不同适应症在国内开启了多项Ⅱ期临床试验,2021年还会有多项临床试验继续开展,这中间还包括一项在美国及澳大利亚开展的二/三线治疗宫颈癌的Ⅱ期临床试验。康方生物预计会在2021年下半年在中国、美国、澳大利亚陆续递交新药上市申请。
目前为止国内还没有双特异性抗体获批上市。但是已经上市的六款PD-1单抗已经表现出了很好的治疗效果,明显提高了免疫治疗市场的成熟度。AK104的适应症范围与PD-1单抗一样广泛,并且有机会达到比PD-1单抗更好的疗效。因此AK104未来的市场空间十分可期。
2.AK105(Penpulimab):联合治疗破局PD-1单抗市场
AK105是康方生物自主研发的PD-1单抗药物。相较于目前已经上市的PD-1单抗,AK105进行了某些特定的程度的改造删除了不必要的功能结构域,使其能更专注于PD-1靶点的功能,因此可以被认为是潜在同类最佳。
在早期临床研究中,AK105就表现出了同类最佳的潜质。在针对R/R cHL(复发性/难治性经典霍奇金淋巴瘤的Ⅰ期临床试验中,5例可评估的患者有3例完全缓解(CR)和2例部分缓解(PR)。
AK105临床研发计划
目前国内已经有6款PD-1单抗上市,包括两款进口产品和四款国产产品。虽然六款产品之间的适应症不完全相同,但是目前为止PD-1单抗的国内市场仍然已经比较拥挤。因此康方生物选择了差异化发展的路线,除了已经有产品上市的经典霍奇金淋巴瘤之外,康方生物将更多的精力投入到了鼻咽癌和联合治疗上。
鼻咽癌是一种明显地域分布不均的癌症类型。在三大人种中,黄种人的鼻咽癌发病率最高。尤其在我国华南地区,鼻咽癌的发病率极高。AK105三线治疗鼻咽癌患者Ⅱ期临床试验已经在2019年3月招募了首名患者,并且CDE已经授予该项试验关键临床试验。康方生物预计将在2021年上半年申请这一适应症的NDA。目前为止还没有PD-1单抗获批用于鼻咽癌治疗,因此AK105可能将成为全球第一款用于治疗鼻咽癌的PD-1单抗。
AK105与化疗联合治疗非小细胞肺癌,表现出了更加出色的疗效。43名可评估的AK105联合用药组受试者有19名出现了部分缓解,ORR达到44.2%。而安慰剂联合用药组的ORR则只有18.2%。
AK105与安罗替尼联合治疗的方案,目前正在肝细胞癌(HCC)和非小细胞肺癌(NSCLC)中进行研究。在肝细胞癌研究中,28位可评估的受试者有6位受试者达到了部分缓解,ORR达到21.4%。
康方生物目前已经与正大天晴成立了一家合资公司,以加快对AK105的开发工作。正大天晴将提供渠道,为康方生物的产品商业化路径保驾护航。AK105与安罗替尼联合治疗预计将在2022年递交NDA。
3.其他产品:聚焦自身免疫病和高胆固醇血症
除了两款核心管线之外,康方生物的其他管线主要集中在自身免疫病和高胆固醇血症,并且已经逐步从临床前阶段向临床阶段过渡。
AK101临床研发计划
AK101是一款靶向IL-12/IL-23的单抗药物,能同时抑制IL-12和IL23与受体之间的相互作用。同靶点药物目前已经有强生的喜达诺(乌斯奴单抗)获批上市,用于治疗斑块型银屑病和克罗恩病。
AK101目前已经完成了针对中重度斑块状银屑病的Ⅱ期临床研究。研究结果表明,接受不同剂量AK101治疗的患者在第12周都有70%以上的患者达到了PASI75(银屑病皮损面积及严重程度指数较基线下降至少75%);另外,接受高剂量(270mg)AK101治疗的患者有58.3%达到了PASI90(银屑病皮损面积及严重程度指数较基线下降至少90%),安慰剂组的相应数字则只在10%左右。
同时AK101在研究中表现出了较好的安全性,虽然有广泛的不良事件发生,但是没有一点严重不良事件发生。最常见的不良事件是上呼吸道感染,而这可能与流感相关。
AK101目前正在进行中重度斑块状银屑病的Ⅱb期临床研究,同时针对中重度溃疡性结肠炎(UC)和系统性红斑狼疮的临床试验也将于2020年陆续开启Ⅰb期临床试验。
AK102临床研发计划
AK102是一款PCSK9单抗,可以降解而降低肝脏清除低密度脂蛋白胆固醇(LDL-C)的能力。目前国内已经有安进的瑞百安(依洛尤单抗)获批上市,用于治疗高胆固醇血症,和动脉粥状硬化,以及降低心血管事件风险。
AK102在健康受试者中进行的Ⅰ期临床试验显示,AK102的耐受性良好,而且能明显降低所有四个剂量组中健康受试者的血脂。
AK102目前正在进行针对纯合子型家族性高胆固醇血症(HoFH)的Ⅱ期临床研究,并且还将于2020年上半年启动有关高胆固醇血症的另一项Ⅱ期临床试验。
AK111临床研发计划
AK111是一款IL17单抗,同种类型的产品已经有诺华的可善挺(司库奇尤单抗获批上市)。AK111在新西兰进行的Ⅰ期临床试验中表现出良好的安全性,于药物相关的不良事件均较轻,而且无严重不良事件发生。预计2020年将有Ⅰb期临床试验在国内开展。
除这些已经处于临床阶段的管线之外,康方生物AK112(PD-1/VEGF)、AK109(VEGFR-2)、AK114(IL-1 beta)、AK119(CD73)、AK123(PD-1/CD73)等多款药物管线即将展开临床试验或已经申请IND。
总的来看,康方生物在目前的管线布局由AK104和AK105两条主力管线牵引,辅以AK101、AK102、AK111等产品做持续的临床开发,后续还包括大量即将开展临床试验或处于临床前阶段的产品。产品分布呈阶梯状排列,主次分明。多款产品同时推进也有利于康方生物抵抗药物研发失败带来的风险。
First in Class新药的市场潜力大,但是相应的研发风险较高;跟随创新药物的市场成熟度高,审批相对容易,但是由市场之间的竞争压力。因此康方生物在新药靶点上选择了多角度同时推进,既有潜在的全球新药AK104,也有在相对成熟的市场中选择差异化竞争的AK105,还包括多款可能成为同类最佳的AK101、AK102、AK111等产品。这样分散投资有利于康方生物控制风险,也凸显康方生物出众的研发能力。
上市融资所得资金将大多数都用在产品研发及商业化
康方生物部分财务数据
由于多条管线的同时推进,康方生物的研发开支即使在创新药企业中也相对较高。2019年度研发开支超过3亿人民币,较上一年几乎翻倍。整体亏损较上一年也同步上升。
康方生物资产情况
在现金储备方面,目前康方生物仍保有人民币12.5元的流动资产总值,但是负债总额较高,可能会造成一定的未来风险。
按照康方生物的计划,2020-2021年,两款主力产品的多个适应症将陆续申报上市。因此可能最早在2021年,康方生物就将有产品获批上市,2022年开始有稳定的产品销售收入。因此康方生物在未来的发展还是比较值得期待。
上市融资资金用途
本次康方生物上市融资所募集的资金,主要(75%)将用于其产品研发及商业化支出。除此之外,有部分资金用于在广州及中山发展生产及研发设施。2020年1月,康方生物在广州的商业化生产基地已经完成封顶,保证康方生物在产品申报上市后可以很快投入市场。
康方生物IPO认购来临,富途4大打新优势
0现金认购:港股/美股/A股通资产抵押,提升购买力,满仓无现金,亦能轻松认购
融资认购:通过融资最高可获得10倍杠杆(即一万本金,可认购10万新股)
超低利率:银行融资认购年利率低至1.6%(具体利率视资金情况微调)
暗盘交易:通过暗盘提前买卖新股
了解更多打新攻略,微信咨询富途渠道商务经理
*封面图片来自:http:///
文 | 郝翰
微信 | hhaaa_bio
转载 授权请联系: kokopellii
声明:动脉网所刊载内容之知识产权为动脉网及相关权利人专属所有或持有。文中出现的采访数据均由受访者提供并确认。未经许可,禁止进行转载、摘编、复制及建立镜像等任何使用。
责任编辑:

